Yoğun bakım tıbbı yeni gelişen teknolojiler ve özellikle de yoğun bakımdaki hastaların bakımIarında standartlann oluşmasını sağlayan klinik çalışmalara bağlı olarak son onyılda belirgin olarak gelişmiştir. 1950’li yıllardaki poliomiyelit epidemisinden buyana yoğun bakım üniteleri akut reversibl hastalıkların tedavisinde önemli faydalar sağlamaktadır. Bununla birlikte yeni gelişen teknolojilerin kullanılması, yakın takip ihtiyacı ve yoğun müdahaleler nedeniyle yoğun bakım tıbbı oldukça pahalıdır ve toplam hastane giderlerinin % 30’unu oluşturur. Yoğun bakım ünitelerindeki (YBÜ) hastalar septik şok ve solunum yetmezliğinden diyabetik ketoasidoz ve üst gastrointestinal sistem kanamalanna kadar farklı tedavi gerektiren değişik hasta gruplannı içerir. Bu yazıda sıklıkla göğüs hastalıkları uzmanları tarafından tedavisi ayarlanan, YBÜ de tedavi edilen hastalıklardan bir kısmı tartışılacaktır. Bu yazının başlıkları akut solunum yetmezliği ve mekanik ventilasyon, akut akciğer hasarı ve şoktur.
Akut Solunum Yetmezliği ve Mekanik Ventilasyon

Akut solunum yetmezliği, tedavi edilmediği zaman ölümcül olan akciğerin yeterli gaz alış verişini devam ettiremediği durumlar sonucu oluşur. Hipoksemik solunum yetmezliği solunum yetmezliğinin oksijenizasyon yetmezliği ile birlikte olduğunu ifade ederken hiperkapnik solunum yetmezliği ventilasyon yetmezliğini ifade eder. Bu hastalıklar parsiyel arteriyeloksijen basıncı (Pa02) ve karbondioksit (PaC02) basıncındaki değişiklikler ile belirgin hale gelirler. Solunum yetmezliğinin tanımlanmasını sağlayan Pa02 ve PaC02 değerleri değişkendir ancak oda havasını solurken Pa02 60 mmHg’nin altında iken veya PaC02 45 mm Hg’nin üzerinde iken solunum baskılanması aşikardır. Kronik akciğer hastalıklarının enfeksiyon, pulmoner emboli, konjestif kalp yetmezliği veya eşlik eden diğer nedenlere bağlı gelişen ataklar sırasında solunum yetmezliği sık olarak görülür.
Bununla birlikte solunum yetmezliği ciddi travma, yoğun sedasyon, nörolojik bozukluk veya diğer birçok duruma bağlı olarak sağlıklı şahıslarda da gelişebilir. Solunum yetmezliğinin tedavisi klinik tabloya bağlı olarak değişir. Solunum yetmezliği olan hasta koopere, uyanık ve hemodinamik olarak stabil ise entübasyon ve mekanik ventilasyon ihtiyacı olmadan gaz alışverişi ve tüm durumların izlenmesinin sağlandığı sürece yoğun solunum tedavisi sağlanabilir. Bu tedavi, PC02 yüksekliğini (85 mmHg’ye kadar) tolere edebilen kronik obstüriktif akciğer hastasına (KOAH) da uygulanabilir. Fakat solunum yetmezliği olan hastalarda ciddi solunum sıkıntısı belirtileri varsa (solunum hızı> 30 solunum /dk vb), mental bozulma (örn., konfüzyon, somnolans, halüsinasyonlar) veya hemodinamik bozukluk varlığında (bradikardi veya taşikardi, hipotansiyon) sıklıkla entübasyon ve mekanik ventilasyon gerekir. Daha da fazla kötüleştiğinde, arteryel kan gazı analizi beklemek gereksizdir ve tedavinin tehlikeli bir şekilde gecikmesine sebep olabilir. Solunum yetmezliği olan hastalarda arteriyel kan gazı analizi mekanik ventilatör ihtiyacını belirlemede hayati olsa da, hastanın klinik durumu hareket planını belirleyecektir. Geri dönüşümlü olduğu düşünülen solunum yetmezliğinde entübasyon ve mekanik ventilasyon geneııikle tercih edilen bir seçenek olsa da KOAH’ lı ve başka hastalığı olan seçilmiş hastalarda noninvaziv pozitif veya negatif ventilasyon yararlı olabilir.
Noninvaziv pozitif basınç, ventilatör ile bağlantılı tam olarak uyumlu maske aracılığı ile sağlanır. Yine de noninvaziv ventilasyon sıklıkla hastanın ihtiyaç duyduğu ventilasyon desteğini sağlamakta yetersiz kalır. Entübasyon kararı alındığında deneyimli bir uzman tarafından entübe edilmelidir. Entübasyonun komplikasyonu sıklıkla işlemin gecikmesine bağlı oluşan uzamış hipoksemidir. Bunun haricinde mide içeriğinin aspirasyonu ve kusma, vokal kord travması, kanama, pnömotoraks, kardiyak aritmiler ve kardiyak arrest diğer komplikasyonlarıdır. Tüp içeri yerleştirildikten sonra bağlanmalı ve solunum seslerinin muayenesi ile pozisyonu ayarlanmalı ve daha sonra akciğer grafisi ile yeri kontrol edilmelidir. Bronkoskopi ile direkt olarak görülmesi nadiren gereklidir. Ventilatör işlem başlatılmadan hazır bulundurulmalı ve işlem biter bitmez mekanik ventilasyona başlanmalıdır.
Mekanik Ventilasyon
Başlangıç ventilatör ayarları değişebilir ancak genellikle asist kontrol modda, inspire edilen oksijen fraksiyonu (Fiüz) 1. O (%100), solunum sayısı dakikada 10-12 solunum ve tidal volüm 400-600 mL olacak şekilde ayarlanır. Ventilatör ayarlarının yeterli olup olmadığı tekrar eden arteryel kan gazı seviyeleri ve hastanın klinik durumunu değerlendirilmesine belirlenir. Devam eden siyanoz, solgunluk, terleme ve solunum sıkıntısı tüpün yanlış yerleştirildiğinin veya ventilatör ayarlarının yetersiz olduğunu düşündürür.
Pozitif ekspiryum sonu basınç (PEEP) dirençli hipoksemili hastalarda gerekli olabilir. PEEP ekspirasyon sırasında alveollerin erken kapanmasını engelleyerek ve ventilasyon perfüzyon dengesini iyileştirerek oksijenizasyonu düzeltir. Ayarlar, arteryel kan gazı düzeylerini göreceli olarak normal (pH 7. 3 -7. 45 arası, PÜz> 6OmmHg, PCüz 30 -45 mmHg arası) değerleri elde edecek şekilde yapılmalı. Solunum yetmezliğinin sebebi ortadan kalkıncaya veya tedavi edilinceye kadar yeterli oksijenizasyonu ve ventilasyonu sağlayacak plan geliştirilmesi konusunda dikkatli olunmalıdır. Bu plan sedasyon ihtiyacını, uygun mekanik ventilasyon stratejisi, beslenme desteği, hemodinamik stabiliteye ulaşmak için destek ölçümleri ve solunum yetmezliği gelişmesine sebep olan başlangıçtaki duruma (pnömoni, pulmoner emboli, astma ve şok gibi) yönelik tedaviyi içermelidir. çoğu hasta rahatsızlık hissini azaltmak ve solunum iş yükünü azaltmak için sedasyon ihtiyacı duyar ancak sedasyon sıklıkla kan basıncında düşmeyle birlikte olduğu için dikkatli olarak kullanılmalıdır.
Günümüzde en sık kullanılan ventilasyon tipi volüm sikluslu veya basınç kontrollü ventilasyon şeklinde verilebilen pozitif basınçlı ventilasyondur. Volüm sikluslu ventilasyonda cihaz üzerinde belirlenen volüm hersiklusta verilir. Bu ayarda inspiratuvar basınç akciğer kompliansına bağlıdır. Bu nedenle yüksek kompliansa sahip hastalarda (ampizem gibi) daha önceden belirlenen volüm daha düşük inspiratuvar basınçlar ile sağlanabilecektir. Bunun tersine düşük komplianslı akciğere sahip hastalar (akciğer fibrozisi veya ödem) aynı volümü vermek için inspiratuvar basınç göreceli olarak daha yüksek olacaktır. Basınç kontrollü ventilasyon kullanıldığında klinisyen belirlenen zamanda inspratuvar basıncı ayarlar. Bu ayarda tidal volüm, sağlanan inspiratuvar basınç ve akciğer kompliansına bağlı olarak değişir. Böylece volüm sikluslu ventilasyonda basınç değişikliklerine rağmen tidal volüm sabit tutulurken basınç kontrollü ventilasyonda inspiratuvar basınç sabit tutulurken tidal volüm değişir. Basınç kontrollü ventilasyon genellikle klinisyen tarafından ventilatörün verdiği basıncı sınırlama konusunda endişesi olduğunda kullanılır.
Pozitif basınçlı, volüm sikluslu ventilatör kullanıldığında birçok mod mümkündür. 1980’ lerde en popüler mod intermittan zorunlu ventilasyon (IMV) idi. IMV ile klinisyen tidal volumü ve ihtiyaca göre solunum sayısını ayarlayabilir. Ventile edilen veya desteklenen solunum, spontan eforla oluşturulan negatif basınçla (genellikle 1-2 cm Hzü) tetiklenir ve valf açılır, önceden belirlenen tidal volüm verilir. Hastanın solunum hızı değişebilir ancak desteklenen solunum sayısı değişmez. Bu mod hastaları ventile etmede yeterli olsa da genellikle spontan ve desteklenen solunumu ayırmada zorlukla karakterize senkronizasyon bozukluğu ile birliktedir. Ek olarak hasta spontan solunumu ventilatörde ayarlanan solunumdan fazla olduğunda spontan solunumlar desteklenmez. Bu iki durum solunum iş yükünde artışa yol açar. Asenkrozisyonu azaltmak için desteklenmiş spontan solunumlar ile senkronize edilebilen senkronize intermitant zorunlu ventilasyon
(SIMV) geliştirilmiştir. Ne yazık ki bu modda desteklenmemiş solunumlar sırasında solunum iş yükü artışı devam eder. Bu kısa geçmişten sonra günümüzde tercih edilen ventilasyon asisted-control (AC) ventilasyondur. (Controllü mekanik ventilasyon (CMV) olarak ta adlandırılır). AC ventilasyonda klinisyen tidal volümü ve izin verilen en düşük solunum sayısı ayarlanır aynı zamanda spontan solunumlarda desteklenir. Diğer taraftan ayarlanmış solunum sayılarından bağımsız olarak tüm solunumlar desteklenir. AC ventilasyonu en fizyolojik mod olarak düşünülür ve diğer volüm siklus veya basınç kontrolü ventilatör modIarına güre en düşük solunum iş yüküne sahip moddur.
Diğer bir ventilatör moduda basınç destek ventilasyondur. Bu mod basınç kontrollü ventilatör ile verilir ve, daha önce bahsedilmişti, klinisyenin inspratuvar basıncı ayarlaması gereklidir. Ventile edilen solunumlar, akımdaki değişikliklerle belirlenen spontan solunumlarile tetiklenir. Daha sonraki tetiklemeler havayı içeri verir fakat verilen volüm ayarlanan basınca ve akciğerin kompliansına bağlı olarak değişir. Bu modda yeterli tidal volmü vermek için klinisyenin inspratuvar basıncı ayarlaması gerekir. Bununla beraber, pratikte, deneyimli bir klinisyenin elinde bu mod ile AC ventilasyon arasındaki fark çok azdır.
Mekanik Ventilasyondan Ayrılma
Mekanik ventilasyonun ve entübasyonu n birçok komplikasyonu vardır; barotravma ve pnömoni en belirgin olanıdır. Böylece mekanik ventililasyon uygulanan hastalar agresif olarak tedavi edilmeli ve dikkatli bir şekjlde izlenmelidir. Mekanik ventilasyondan ayırmada, solunum yetmezli düzeldiğinde özellikle hasta uyanık, koopere ve solunumsal veya hemodinamik insitabilite bulgusunun olmadığı hastalarda düşünülmelidir. Şayet destek oksijen miktarı yüksekse (Fi02 O. S’den fazla ise) weaning düşünülmemelidir. Weaningin başarılı olup olmayacağını belirlemede konvansiyonal parametreler; negatif inspirator güç, vital kapasite, tidal volüm, solunum hızı, ve dakika ventilasyonudur. Bu parametrelerin weaning yetersizliğini tahmin etmede spontan solunum başarısını tahmin etmeye göre daha başarısızdır. Weaning kapasitesini belirlemede en iyi yol ventilasyon desteğini azaltarak hastanın kısa weaning denemeleri yapmasını sağlamaktır. Bu denemeler basınç desteği sağlamadan T tüp yardımı ile 1 saat boyunca hastanın oksijen solumasıyla gerçekleştirilebilir. Diğer bir strateji ise devamlı pozitif havayolu basınç (CPAP) denemeleri sırasında ventilatörün ürettiği basıncın aza1tılmasıdır. Hastada herhangi bir solunum sıkıntısı bulgusu veya hemodinamik instabilite izlenmeli ve spontan solunumun etkinliğini belirlemede tekrar eden arteryel kan gazı ölçümleri yapılmalıdır. Hasta bu denemeleri tolere ederse hastanın klinik durumu ve alta yatan hastalığın durumuna göre ekstübe edilebilir. Genellikle bu denemeler sonrası ekstübe edilen hastaların %LO -% iS’ inde tekrar entübasyon gerekebilir. Şayet hasta weaning denemelerinde başarılı olamaz ise weaning yetmezliğine yol açan durumlar belirlenmeye çalışılmalıdır. Sıklıkla bütün belirgin ek durumlar belirlenebilir ve düzeıtilebilir ancak ekstübasyondan önce daha uzun weaning denemeleri gerekir. Bu ayarlamada iki weaning stratejisi önerilmektedir. ilki genelikle AC ventilasyon yoluyla verilen ventilatuvar destek sırasında günde 1 veya iki kez hastanın T tüb yardımı ile spontan solunumlar yapmasıdır. Diğer strateji ise basınç destek ventilasyonu kullanımına bağlıdır. Ventilatör SIMV modu sırasında düşük solunum hızında ayarlanır ( genellikle 6 solunum dakşkadan daha az) ve hasta solunum desteği solunum yapıncaya kadar inspratuar basınç progresif olarak azaltılır. Uzamış mekanik ventile edilmiş kronik akciğer hastalığı olan hastalarda weaning için basınç destekli ventilasyon öneriIse de bu iki stratejinin etkinliği birbirine yakın gibi görünmektedir.
Akut Akciğer Hasarı
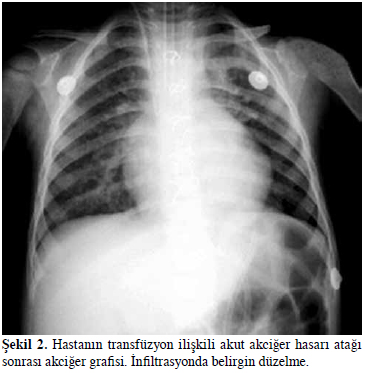
Akut diffüz akciğer hasarı ve onun en ciddi formu akut solunum sıkıntısı sendromu (ARDS) olarak adlandırılır. Akut akciğer hasarı alveola kapiller membranın geçirgenliğinin artması sonucu alveolar boşluğun proteinden zengin materyal ile dolması ile oluşur ve ARDS akciğer yetmezliğinin klinik olarak ciddiyetinin (Pa02/Fi- 02 gibi) ölçülmesiyle tanınır. Bu durum aspirasyon pnömonisi, duman inhalasyonu, boğulayazma gibi direkt hasar ile veya travma, cerrahi, sepsis, yanık, uzun kemik kırıkları, pankreatit, üremi, transfüzyon tedavisi, şok, ilaç toksisitesi, veya kardiopulmoner bypass gibi sistemik hasar ile tetiklenebilir. ABD de yılda yaklaşık 150000 ARDS vaka sı bildirilmektedir. Aspirasyon pnömonisi ve sepsis en sık alta yatan sebeptir. ARDS ye bağlı mortalite oldukça yüksektir ve yaklaşık %40- %50 hasta ölür. ARDS, hasara enflamatuar anormal yanıt sonucu oluşan sistemik hastalığın akciğer tutulumudur.
Kontrolsüz enflamatuar yanıt, her iki fizyolojik bariyerde geçirgenlik artışına yol açan pulmoner vasküler endotelde ve epitelde hasar meydana getirerek intravasküler alandan proteinden zengin sıvının sızmasına izin verir ve sıvı akciğer interstisyumunda ve alveolar boşlukta birikir. Bu durum nonkardiyojenik akciğer ödemi olarak tanımlanır. Akciğerde bu süreç dirençli hipoksemiye ve akciğer kompliansında azalmaya yol açar, böylece solunum iş yükü artar. Diğer organ yetmezlikleri sıktır, sonuç olarak özellikle sepsiste multiorgan yetmezliği yaygındır.
Yaygın akciğer hasarı ile birlikte olan hyalin membranlar ARDS’nin karakteristik histolojik bulgusudur. Sürfaktan sentezi miktarında ve fonksiyonunda azalma sonucu oluşan atelektaziler oluşan hasarı artırır. Birkaç gün sonra dokuda tip II pnomositlerde hiperplazi ve bağ dokusu materyallerinde birikim sonucu fibrozis oluşur. Mekanik ventilasyondaki pozitif basınç, hiperdistansiyon ve hiperoksi sonucu bu olaylar daha da kötüleşebilir. Altta yatan hastalığı olan hastalarda (sepsis vb), bilateral pulmoner infiltrasyonlar ve dirençli hipoksemi (genelikle Pa02/Fi02’nin 200 mmHg ve daha düşük) varlığında ve kardiyak bozukluk bulguların olmadığı zaman ARDS tanısı düşünülmelidir. Günümüzde ARDS tedavisi hasara sebep olan ajan eradike edilinceye kadar kardiyovasküler ve beslenme desteği ve enfeksiyon ve barotravma gibi komplikasyonları önlenmesi gibi destek tedavisidir. Son zamanlarda ventilatör destek tedavisi ayarları düşük tidal volüm de (6mL/kg) verilmektedir. Bu tedavi şekli daha yararlıdır ve sağkalım artmıştır. Kortikosteroidler, sürfaktan tedavisi ekstrakorporyal oksijenizasyon faydalı değildir ve önerilmemektedir. Oksijenizasyon pron pozisyonu ve PEEP ile artınlabilir ancak bu uygulamalar hastalığın doğal seyri üzerine etki etmez. İnspire edilen havaya nitrik oksid eklenmesinin etkileri araştırılmış ve ARDS tedavisinde gerçek etkileri tam olarak belirlenememiştir
Sistemik Enflamatuvar Yanıt Sendromu

Sistemik enflamatuvar yanıt sendromu (SIRS), çeşitli sebeplere karşı konağın cevabıyla oluşturulan klinik Şok; genellikle hipotansiyonun eşlik ettiği hücre hasarı ve ölümüne yol açan sistemik organ hipoperfüzyonu olarak tanımlanır. Dört sınıflama vardır.1 Kardiojenik şok (işlev bozukluğuna yol açan kardiyak outputta azalma) 2 Hipovolemik şok (intravasküler volümde azalma) 3 septik veya redistribüsyon şok (sistemik vasküler dirençte azalma) veya 4 obstrüktif şok (akımda tıkanıklığa yol açan kardiyak outputa azalma) (ilaçlara veya ilişkili diğer durumlara bağlı allerjik reaksiyon sonucu oluşan anafilaktik şok olarak bu bölümde tartışılmayacaktır). Şoklu bir hastayla karşılaşıldığında mevcut durumu dikkatlice değerlendirirken en kısa zamanda damar girişi sağlanarak yoğun volüm replasmanı sağlanmalıdır. Bu tedavi stratejisi şokun sebebi hipovolemik veya sepsise bağlı olduğu düşünülüyorsa daha faydalı olacaktır. Kardiyojenik şokta tedavi stratejisi inotroplarla veya yanıt alınamayan ciddi vakalarda kardiyak bypass ve kardiyak destek cihazlarıyla yapılmalıdır. Ciddi hipovolemide salin infüzyonu yeterli olabilir fakat bazan kolloid (kan, albümin) uygulanması gerekli olabilir. Septik şokta sıvı tedavisi, antibiyotik tedavisi ve herhangi bir enfekte alanın drenajı en iyi yoldur. Erken teşhis edilmiş ciddi sepsisli seçilmiş hastalarda rekombinant aktive protein C’nin (drotrecogin alfa (aktive)) intravasküler uygulanması ile sağkalırnda iyileşme gösterilmiştir. Obstürüktif şok; kan akımındaki obstrüksiyona yol açan masif emboli veya sağ ve sol pulmoner arterin bifurkasyon yerindeki eğer tarzdaki emboli ile meydana gelir.
Bu durumda obstrüksiyonun mekanik veya diğer yöntemlerle (trombolitik) eliminasyonu veya obstrüksiyon önemli ise hastanın dolaşımı desteklenmelidir. Şokun tedavisinde kan basıncının ve organ perfüzyonunun takibi çok önemlidir. Santral venöz kateter ile yeterli sıvı tedavisi verilebilir ve kesin kan basıncı ölçümü için arteryel kateterizasyon yapılabilir. Yoğun sıvı tedavisinin etkili olmadığı ve şoku n sebebi tam olarak bilinmiyorsa pulmoner arteryel kateterizasyon (Swan-Ganz) yaralı olabilir. Bu katater ile sağ atrium, sağ ventrikül, pulmoner arter ve pulmoner kapiller kama basıncı direkt olarak ölçülebilir ve kardiak output değerlendirilmesi yapılabilir. Bu değerler ile kardiyak indeks, sistemik ve pulmoner direnç, ve oksijen içeriği gibi değerlerin hesaplanmasında kullanılabilir. Bu katater ile elde edilen ve hesaplanan parametreler Tab Bu kateterin yerleştirilmesi ve elde edilen verilerin yorumlanması belirgin deneyim gerektirir.
Pulmoner enfeksiyonlar yıllık 6 milyon insanı etkilemektedir; pnömoni ABD’de ölümlerin en sık 10 nedeninden birisidir. Pulmoner enfeksiyonlar virüs, bakteri ve funguslar gibi çeşitli organizmalara bağlı olabilir. Hastalar sıklıkla prodüktif öksürük, dispne, göğüs ağrısı ve bazende hemoptizi tarif ederler. Diğer nadir spesifik semptomlar ateş, genel düşkünlük, kas ağrısı ve kilo kaybıdır. Hastalık bakteriyel pnömonilerdeki gibi akut (günlük yada haftalık) veya tüberkülozdaki gibi subakut yada kronik (haftalar yada aylar) olabilir. Altta yatan (örn., HIVenfeksiyonu) gibi hastalığı olanlar spesifik hastalığa yatkın olabilirler ve konakçı defansındaki spesifik bozukluğun mekanizmasını bilmek enfeksiyon etkenini saptamakta yardımcı olur. Tanı ve tedavi klinik, görüntüleme ve laboratuvar bulgularına dayanır.
Bunların içinde akciğer radyografisi önemli roloynar. Parankimal opasite hastanın pnömoni olduğunu düşündürür, bununla beraber nonenfeksiyöz hastalıklarda pnömoniyi taklit edebilir ve hiçbir radyografik bulgu enfeksiyon için tamamen spesifik değildir. Bir parapnömonik enfüzyon da mevcut olabilir.
Hastayı pnömoni olarak değerlendirirken özel lokalalizasyondaki enfeksiyöz organizmaların epidemiyolojisini iyi anlamak ve hastanın konakçı savunma mekanizmalarının gücünü bilmek tedavi için yol gösterici olabilir. Streptococcus Pneumonia bütün pnömonilerin %26’sı ve toplum kökenli olanların %60-75’inin nedeni olan gram (+) diplokokal bir bakteridir. S.pneumonia kapsüllü olduğunda (örn., Serotip 3) yüksek mortalite riski taşır. Etkilenen hastalar sıklıkla yaşlı erişkin, immünkompromise hastalar ve alkol kullananlardır. Hastaların öncesinde bir üst solunum yolu enfeksiyonu olabilir ve bunu ateş, titreme, plörezi izler. Öksürük prodüktif ve pürülandır ve paslı balgam sık görülür. Görüntülerne çalışmaları alveoler konsolidasyonu gösterir. Bakteriyemik vakaların sadece %45’inde balgam gram boyama pozitif sonuç verir. Bundan dolayı organizmaların kan, plevral sıvı ve serebrospinal sıvı gibi steril yerlerden alınması tanıyı doğrular. Klinik pratikte, tanı muhtemeldir. Ampirik tedavi başlandıktan sonra invaziv tanı yöntemleri nadiren gerekir. Penisilin G ve eritromisin ilk seçenek ilaçlardır. Bununla beraber penisilin, eritromisin trimetoprim-sulfometoksazola dirençli streptomisin tipleri artmaktadır. Böylece 2. ve 3. jenerasyon sefalosporinler, yeni makrolidler (örn., Azitromisin ve Klaritromisin) ve kinolonlarda (örn., Levaquin, Tequin) tedavi seçenekleridir. Antibiyotikler tedavi başladıktan 5 gün sonra hastaların çoğunda ateş düşer fakat radyografik düzenleme 14 güne kadar, hatta erişkinlerde daha uzun sürebilir. Mycoplasma pneumonia yavaş üreyen, fakültatif anaerobik bir organizmadır ve atipik pnömonilerin %25- 60’ına neden olur. Mycoplasma pneumonia 5-35 yaş arası öncesinde üst solunum yolu semptomu, farenjit ve büllöz mirinjiti olan hastalarda görülür. Kuru öksürük, ateş, gastrointestinal semptomlar, baş ağrısı ve miyalji sıktır.
Akciğer radyografisinde hava bronkogramları içeren konsolidasyona ilerleyebilen intersitisyel retikülonodüler infiltratlar görülür. Plevral efüzyonda görülebilir fakat hiler genişleme nadirdir. Tanı zordur ve klinik ve epidemiyolojik özelliklere dayanır. Akut ve konvelesan serolojik bulgular tanıyı desteklemek için gereklidir fakat akut hastalık döneminde yardımcı değildir. Soğuk aglutininler nonspesifiktir ve kültürün üremesi 2 ile 3 hafta almaktadır. Enzim bağlantılı immünosorbent çalışması (ELISA) ve DNA problarının hibridizasyon ile birleşmesini içeren yeni teknikler daha hızlı ve dayanıklıdır. Tedavi için makrolidler önerilmektedir.
Nozokomial pnömoni hastaneye yatıştan 72 saat sonra oluşan bir pnömonidir ve hastane kaynaklı enfeksiyonların en sık ikinci nedenidir. Nozokomial pnömoni ciddi marbidite ve mortalite ile ilişkilidir; nozokomial enfeksiyonlarda en sık ölüm nedeni pnömonidir. Mekanik ventilatör nozokomial pnömonide en güçlü risk faktörüdür ve bu hastalık ventilatör ilişkili pnömoni (VAP) olarak adlandırılır. Özellikle entübasyondan sonraki ilk dört gün içinde VAP’a yol açan bakteriyel patolojenler Streptococcus pneunıonia, Hemophilus inj7.uenza, Moraxella catarrhalis’tir. Daha sonra VAP’a Pseudonıonas aeruginosa, Acinetobacter sp., Enferobacfer sp., ve Staphylococcus aureus neden olur. Nozokomial pnömoni insidansı genel cerrahide % 10, yoğun bakım ünitesinde %20 ve akut respiratuar yetmezlik sendromunda %70’dir. Birçok nozokomial pnömoniler polimikrobialdir ve gram (-) basil, aerob ve Staphylococcus sp.'yi içerir. Gram (-) basiller P.aeruginosa ve metisilin dirençli stafilokoku içerir. Legionella sp.'de nozokomial pnömonilerde artışlardan sorumlu önemli patojenlerdir. Nozokomial pnömoninin patogenezinde orofarinks ve midenin virulan patojenler ile kolonize olması ve bu organizmaların alt solunum yollarına aspire edilmesi vardır.
Gram (-) organizmalar ile gastrik kolonizasyon gastrik asidin nötralizasyonu tarafından arttırılır. Diğer risk faktörleri, eş zamanlı hastalıklar, beslenme alışkanlığında bozulma, invaziv tedavi edici müdahaleler, sigara öyküsü, ileri yaş, ev hemşiresi bakımı ve mekanik ventilasyonu içerir. Tanı için klinik kriterler göreceli olarak azdır, radyografik bulgular nonspesifiktir ve sıklıkla multilober infiltratlar ve efüzyonu gösterir. Multiple kaviteli nodüler infiltrasyonlar stafilokok septik embolisi için anlamlıdır. Nozokomial pnömoni teşhisi bronkoskopik lavaj veya endobronşial fırçalamadan alınan steril örnekleme kültürü ile arttırılabilir.
Tedavi kombine kemoterapiye dayalıdır ve beta laktam antipsödomonal penisilin veya sefalosporin ile birlikte aminoglikozit veya kinolonu içerir. Metisiline dirençli Sfaphylococcus sp. saptanırsa vankomisin eklenir. Eğer şiddetli şekilde aspirasyon pnömonisi düşünülüyorsa Klindamisin ve ilişkili ilaçlar kullanılabilir. Aerobik, hareketsiz, niasin üreten asit-fast çomak olan mycobacterium tuberculosis enfeksiyonu tüberküloza neden olur. World Health Organization Global Surveillance and Monitoring Project 1997’de yılda 8000000 yeni tüberküloz vakası olduğunu hesaplamıştır ve enfeksiyonların 3,5 milyonu akciğer hastalığını içerir. Ek olarak 16,2 milyon hastalıklı vaka da yaşamaktadır. Her yıl 1,87 mjlyon kişi tüberkülozdan ölmektedir ve global vaka HIV nedenjnden ötürü oran %50’dir. ABD’ de 1990’ların başında tüberküloz, HIV enfeksiyonundaki artış, ilaç suistimali ve iç şehirlerde yoksulluk ve evsizliğe bağlı
olarak alarm seviyesinde artmıştı. Enfeksiyon doğrudan basil ihtiva eden damlacığın inhale edilmesiyle kazanılır ve basil hücre içi çoğalmanın gerçekleşeceği alveoler makrofajlar tarafından yutulur ve bunu ölü hücrelerde basilin serbest kalması takip eder. Enfeksiyonun hapsedilmesi T lenfosit ve makrofajlar arası koordinasyonu gerektiren spesifik hücresel immüniteye bağlıdır. Histolojik olarak M.tuberculosis ile enfekte olmuş dokularda kazeifikasyon veya nekroze olmuş granülomlar saptanır. Bu konakçı defans mekanizması HIV’ı olanlarda bozulur ve granülomlarda zayıf gelişmelere neden olur.
Hastalarda haftalar yada aylarca süren sinsi semptomlar olabilir. Ateş, kilo kaybı, gece terlemesi ve prodüktif öksürük sıklıkla görülür. Akciğer radyografisinde üst lobların apikal ve posterior segmentlerinde kavitasyon ile yamalı infiltratlar görülür. Bronkojenik yayılım ile enfekte materyal alt loblara yayılır. Akciğer radyografisinde milier patern görülebilir ve bu hematojen yayılımın göstergesidir. Atipik görünümler ile yaşlı erişkin lerde ve immünsüprese sistemi olan hastalarda karşılaşılabilir.
Mycobacterium tuberculosis enfeksiyonunun tanısı aktif hastalığı değil fakat temas veya eski enfeksiyonu gösteren pozitif tüberkülin testine dayanır. Tüberkülin A dönüşümünden sonra erken safhada aktif tüberküloz için hastalar yüksek risk altındadır ve bu da profilaksinin gerekliliğini özellikle dönüşümden sonraki 2 yıllık sürede göstermiştir. Profilaksi, yetersiz tedavi öyküsü olanlarda veya 35 yaş altında pozitif tüberkülin reaksiyonu olanlarda gereklidir. İmmünkompromise sistemi olan hastalarda radyografik olarak eski inaktif tübekülozu olanlar i yıllığına tedavi edilebilir. Profilaksi, İzoniazid 300 mg ile 6 ile 12 aylığına yapılır. Aktif hastalık olduğundan şüphelenildiğinde en az 4 ilaç içermelidir; İzoniazid 5 mg/kg/gün; Rifampin 10mg/kg/gün; etambutol 5-25 mg/kg/gün; pirazinamid 15-30mg/kg/gün, ve öncesinde resmi tanı yöntemleri yapılmalıdır. (örn., Tüberküloz teması, pulmoner semptomlar, görüntüleme çalışmalarında kaviter hastalık olması) Tanı teyit edildiğinde ilaçlara 2 ay devam edilmeli ve ilaç tedavisinin yan etkileri izlenmelidir. İki aydan sonra ilaç duyarlılık çalışmalarına dayanarak 4 ay daha en az 2 ilaçla devam edilmelidir. Basili tanımlamak veya klinik örneklerin kültürde üremesi (örn., balgam, bronkoalveoler lavaj, doku) tüberküloz tanısını onaylar. İlaca dirençli tüberkülozun oranı belli popülasyonlarda artmaktadır (örn., İspanyol, Güneydoğu Asyalılar).
Direnç daha önce tedavi almamış hastalann %9’unda ve öncesinde tedavi alanların %22,8’inde saptanır. ilaca dirençli tüberkülozu olan hastalarda tedavi daha önce verilmemiş invitro olarak organizmaların duyarlı olduğu en az 3 ilacı içermelidir. Tedavi en az 18-24 ay devam etmelidir. Tedavinin direk olarak gözlemlenmesi uyum garantisi için gereklidir.
Pneumocystıs Carinii fırsatçı bir mantardır ve sıklıkla malnütrisyonlu prematüre bebeklerde ve pre-AIDS çağındaki kemoterapi alan hematolojik maligniteli erİşkinlerde görülürdü. Fakat bunun insidansı 1980’lerin sonları ve 1990’larda düşük CD4 lenfosit sayısı (2S0’nİn altında) olan AIDS hastalarının artışıyla yükseldi. Hastalar nonprodüktif öksürük, ateş, dispne ve kilo kaybından yakınırlar. HIV ile enfekte hastalarda semptomlar haftalar içinde yavaşça ilerler. Oral kandidiazis, yükselmiş serum laktik dehidrogenaz yüksek Aa-oksijen gradienti ve düşük CD4 + miktarı HIV ilişkili Pneumocystls Carinii için bağımsız göstergelerdir.
Toplum yada hastane kökenli akciğer enfeksiyonu yüksek morbidite ve mortalite kaynağı olmaya devam edecektir. Bu enfeksiyonların önemli bir oranı uç yaşlarda çocuklar ve yaşlı erişkinleri etkilemektedir. Endüstri daha yüksek güvenlik ve etki profiline sahip yeni antibiyotik araştırmaya devam etse de ajanların tedbirli kullanımı yeni ajanlar geliştirilene kadar direnç gelişimini önleyecek yada erteleyecektir. influenza gibi ajanlar için güçlendirilmiş aşıların geliştirilebilmesi için devamlı çalışmaya ihtiyaç vardır.



