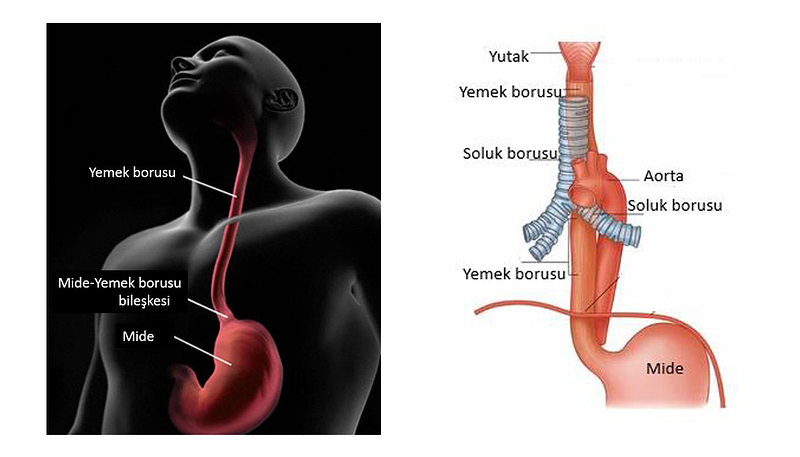
Özefagus karsinomu tüm kanserler içinde en ölümcül olanıdır. Özefagus lenfatik akımının zengin ve iki yönlü olması kadar serozal bariyer ve erken belirtinin olmayışı genellikle geç tanı konulması ile sonuçlanır. Amerikan Kanser Birliği (American Cancer Society) Amerika Birleşik Devletlerinde 2006 yılında yaklaşık olarak 14.550 yeni özefagus kanseri vakası ve 13.770 tane de özefagus kanseri nedeni ile ölüm görüleceğini tahmin etmektedir. Eskiden özefagus kanserlerinin %95’ini skuamoz hücreli karsinom (SCC) oluşturmaktaydı. Bununla birlikte 1980’lerden beri özefagusun adeno karsinomunun insidansı hızla artmıştır ve şimdi yeni tanı konan özefagus karsinomlarının yaklaşık %50’sini adenokarsinom oluşturmaktadır. Özefagus adenokarsinomunun epidemiyolojik mekanizmaları SCC’den farklıdır ama belirtileri, tedavileri ve prognozu birbirine benzerdir.
Dünyada SCC insidansı dramatik olarak değişmektedir. En yüksek oranlar Latin Amerika’nın bazı bölümleri ve Çin, İran, Zimbabwe gibi gelişmekte olan ülkelerde bulunmaktadır. Yıllık 100.000’de 5 insidans oranına bakıldığında, SCC Amerika Birleşik Devletlerinde nispeten daha azdır. Özefagus kanseri 40 yaşına kadar nadirdir ama her on yılda insidansının arttığı bilinmektedir. Erkekler kadınlardan daha sık etkilenmektedir ve diğer ırk ve etnik gruplarla karşılaştırıldığında siyahlarda beş kat fazla görülmektedir. SCC’nin nedeni bilinmemektedir fakat çevresel, beslenme ve özefagusla lokal olarak ilgili faktörler olabileceği düşünülmektedir. Ağır alkol tüketimi ve sigara içme ABD’de SCC için predominant risk faktörleridir. Gelişmekte olan ülkelerde beslenme bozuklukları (mesela selenyum eksikliği), hurma çiğneme (betel nut chewing), human papillomavirus enfeksiyonu, çok sıcak içeceklerin tüketimi (örneğin çay), nitratlar ve turşular da önemli risk faktörlerindendir. Altta yatan durumlar, korozif madde darlıkları, radyasyon yaralanmaları, Plummer Vinson sendromu, akalazya, nasırlaşma ve çölyak hastalığıdır.
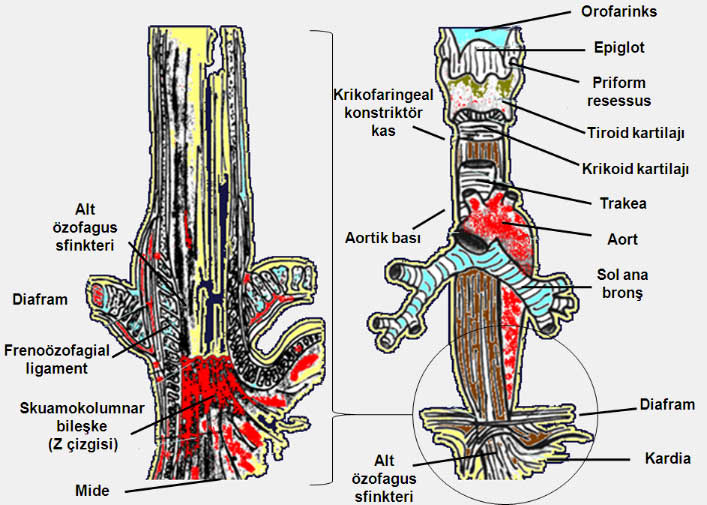
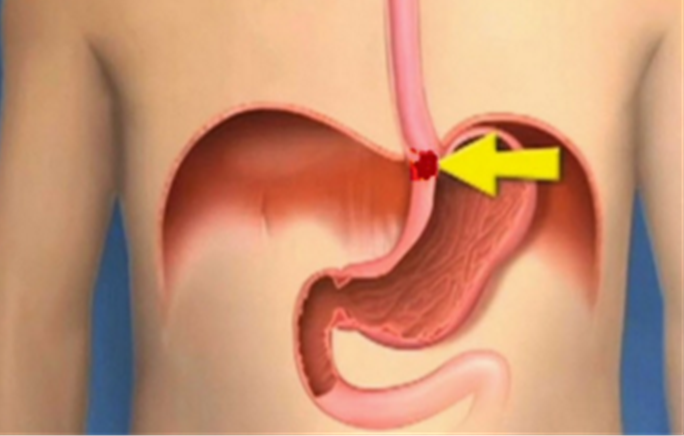
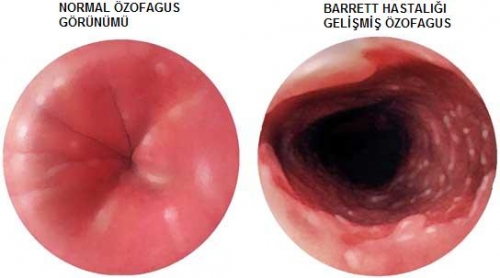
Özefagus adeno karsinoması primer olarak beyaz erkeklerin hastalığıdır. Adeno karsinomanın primer risk faktörü "Barrett özefagusu"dur. Barrett özefagus u kronik gastroozefageal reflüye yanıt olarak intestinal tip kolumnar mukozanın normal squamoz mukozanın yerini alması ile karakterizedir. İntestinal metaplasinin önce düşük dereceli (gradeli) displaziye sonra yüksek gradeli diplaziye ve nihayet adenokarsinomaya dönüştüğü varsayılmaktadır. Barrett özefagusu üzerinde adenokarsinoma gelişme riski yaklaşık olarak yılda 0.5%’ dir. Uzun süren gastroözefageal hastalık, obezite ve sigara içme de potansiyel nedenler olarak bilinmektedir. Barrett özefagusunda endoskopik inceleme ile biyopsi alınması önerilmektedir. Ama bu öneri gastroözefageal reflü için geçerli değildir.
Erken ve tedavi edilebilir özefagus karsinoması genellikle asemptomatiktir ve şans eseri ortaya çıkar. Semptom varlığı hastalığın ilerlemiş ve genellikle tedavi edilemez bir aşamada olduğunun göstergesidir. Dikkatli bir sorgulama ile, hastaların çoğunda belirtilerin tıbbi yardım arayışlarından birkaç ay önce çıkmış olduğu görülür. Özefagus lümeninin normal çapının yaklaşık olarak 75% i tutulduğunda ortaya çıkan disfaji özefageal karsinomanın en sık belirtisidir. Katı yiyecekleri yutma güçlüğünün peşinden sıvılarla da disfaji olmaya başlar. Tamamen tıkandığında, reguıjitasyon, aspirasyon, ve öksürük veya pnömoni meydana gelebilir. Pulmoner semptomlar trakeoözefageal fistül varlığında da ortaya çıkabilir. Tüm hastalarda anoreksi ve kilo kaybı olur. Göğüs ağrısı, hıçkırık, ses kısıklığının olması mediasten, diyafram ve rekürren laringeal sinir gibi komşu yapıların da tutulumunu gösterir. Gastrointestinal kanama olursa, genellikle gizli kanamadır ve demir eksikliği anemisine yol açar. Tümor büyük damarları tutmuşsa hayati tehlike yaratan gastrointestinal kanamalar meydana gelebilir. Çomak parmak, hiperkalsemi ve Cushing Sendromu gibi paraneoplastik sendromlar nadiren görülür.
Disfaji ya da diğer anlamlı belirtileri olan hastalar üst endoskopi veya çift kontrast özefagus baryum çalışması ile değerlendirilmelilerdir. Endoskopinin avantajı biyopsi ya da brush sitolojik çalşma ile kanser dokusu alma fırsatı vermesidir. SCC’nin %50’si özefagusun orta 1/3’ündedir ve diğer %50’si de distal ya da proksimal özefagusta dağılmışlardır. Adenokarsinomaların %90’ı özefagusun distalinde ortaya çıkmaktadır. Göğüs ve karnın CT incelemesi lokal yapıların invasyonunu ve akciğer ve karaciğer metastazlarını araştırmak için yapılır. Özefagus duvarını beş tabakalı yapı olarak gösteren endoskopik ultrasonografi (EUS) tümör derinliğini, lokal invazyonu ve bölgesel lenf nodu tutulumunu saptamada CT’den daha hassastır. EUS şüpheli durumlarda ince iğne aspirasyonu fırsatı da verir.
Özefageal kanseri olan hastaların iyileşmesinde prognozu gösteren en önemli etken evredir ve tedavi seçeneklerini de etkiler. Evreleme tümör-nodül-metastaz sınıflamasına göre (TNM) yapılmaktadır. Sadece özefagus duvarına lokalize tümörler cerrahi olarak tedavi edilebilir. Bununla birlikte küratif rezeksiyon yapılan hastalarda 5 yıllık sağkalım oranı %5-20’ dir. Ameliyat öncesi çok ilaçlı kemoterapi ve buna eklenmiş radyoterapi lokal rekurens oranlarını azaltıp sağkalımı iyileştirebilir. Cerrahi tedaviyi reddeden ya da tıbbi nedenlerle lokal rezeksiyon yapılamayacak hastalar için de kemoterapi ve radyoterapi önerilmektedir. Metastazı olan hastalarda disfaji için palyatif tedavi uygulanmalıdır. Endoskopik yöntemlerle lokal tedavisi (mesela malign darlığın genişletilmesi), endoprotez yerleştirilmesi (stent) ve lazer ya da fotodinamik terapi ile tümör ablazyonu hızlı palyatif tedavi seçenekleridir. En uzun süreli palyasyon kemoterapi ve radyoterapi kombinasyonu ile sağlanmaktadır.
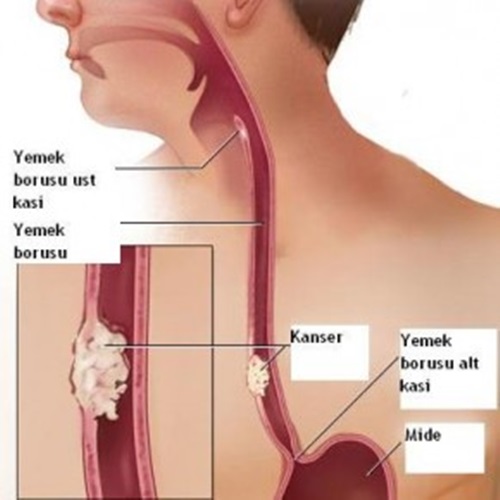
Tüm dünyada kansere bağlı ölümlerin en sık nedeni gastrik karsinomadır. ABD’de mide kanseri insidansı 1930’lardan beri bilinmeyen bir nedenle dramatik olarak azalmıştır. İnsidansın düşmesine rağmen, Amerikan Kanser Birliği (American Cancer Society)'nin tahminlerine göre 2006 yılında yaklaşık 22.280 yeni vaka ortaya çıkması ve mide kanseri nedeni ile 1.430 ölüm vakası görülmesi beklenmektedir. Ne yazık ki mide kanseri tanı konulduğunda genellikle ileri aşamadadır ve 5 yıllık sağkalım %5 ile %15 arasındadır.
Mide kanserlerinin %90’dan fazlasını adenokarsinomlar oluşturmaktadır. Mide kanseri insidansı dünyada büyük farklılıklar göstermektedir. Hastalık endüstrileşmiş ülkelere göre gelişmekte olan ülkelerde daha sıktır ve şehirli ve düşük sosyoekonomik gruplarda daha çok görülür. En yüksek oranlar Japonya, Çin, Güney Amerika ve Doğu Avrupa için saptanmıştır. En düşük insidans oranları yüzbinde on vakadan daha düşük olarak ABD’dedir. Mide kanseri 40 yaşın altında nadiren görülür; bu yaştan sonra da düzenli olarak artar ve 70’li yaşlarda pik yapar. Bu oran kadınlara oranla erkeklerde yaklaşık olarak iki kat kadar fazladır. Zencilerde, Hispanik ve Native Amerikalılarda mide kanseri beyazlara göre 1.5-2.5 kat daha fazla görülür. Hastalıkta çevresel faktörlerin önemli rol oynadığını gösterir bir bulgu olarak, göçmenlerde risk oranları göç ettikleri ülke ile benzerdir. Düşük sosyo ekonomik düzey, besinlerin uygunsuz saklanması ve diğer diyetle ilgili ve lokal gastrik faktörler hastalıkla ilişkili bulunmuştur. Diyetle ilgili faktörler yağ protein ve A ve C vitaminIeri eksikliği, salamura et ve balık ve nitratlardır. Atrofik gastrit, postgastrektomi durumları, aklorhidri, pernisyöz anemi, adenomatöz polipler ve Menetrier’s hastalığı gibi altta yatan durumlar da insidansı artırabilir.
Dünya Sağlık Örgütü Helikobakter Pilori’yi bir kanserojen olarak sınıflar ve epidemiyolojk olarak gastrik adenokarsinom ile ilişkili olarak bildirir. Bununla birlikte, H. Pilori saptanan hastaların çok küçük bir kısmında gastrik adenokarsinom gelişmektedir. Gastrik lenfomalar primer gastik malignitelerin %5’inden daha azını oluşturur. Mide ekstranodal non-Hodgkin’s Lenfomanın ençok görüldüğü bölgedir ama midenin Hodgkin lenfoması nadirdir. Gastrik mukozanın lenfoid doku (MALT) lenfomaları %90 vakada H. Pilori ile ilişkilidir ve H. Pilori eradikasyonundan sonra %60-70 vakada gerileme görüldüğü bildirilmektedir. MALT Lenfomaları bir çok otoimmün ve immün yetmezlik sendromlan ile de ilişkili olarak görülebilir. Bu lenfomaların çoğu 50 yaş üzerinde ortaya çıkar ve erkeklerde biraz daha fazla olduğu bilinir.
Gastrik malignitelerin yeri, büyüklüğü ve büyüme şekli ortaya çıkan belirtileri etkileyebilir. En sık belirti karında rahatsızlık hissidir; bununla birlikte özellikle mide Çıkışı tıkandığında erken doyma, bulantı ve kusma görülebilir. Gastrointestinal kanama demir eksikliği anemisi, gizli kanama veya açık bir üst gastrointestinal kanama şeklinde olabilir. iştahsızlık ve kilo kaybı sıklıkla diğer belirtilere eşlik eder. Fizik muayenede ortaya çıkabilecek ve tedavi edilemezlik olasılığına işaret eden metaztatik hastalık belirtileri; Virchow nodülü (sol supraklaviküler), Blumer’s shelf (dijital rektal incelemede saptanan perirektal poş içinde kitle) ve Krukenberg tümörü (over metastazı)dür. Birçok paraneoplastik sendrom gastrik adenakarsinama ile ilişkilidir ve gastrointestinal malignite araştırması yapmayı gerektirir. Bunlar Trousseau’s Sendromu (tromboz), Akantasis Nigrikans (pigmente cilt lezyonları), membranöz nefropati, mikroanjiyopatik hemolitik anemi, Leser- Tre iat belirtisi (seboreik keratoz) ve dermatomiyozittir.
Gastrik malignitelerin tanı testleri çift kontrast üst gastrointestinal radyografi veya endoskopidir. Baryum çalışmasında gözlenen lezyonlardan histolojik değerlendirme için sitolojik çalışma yapmak ve endoskopik biyopsi almak gerekir. Gastrik karsinamalar ülser, kitle, mide katIantılarında büyüme veya, esnek olmayan mide duvarına infiltrasyon (linitis plastica) şeklinde görülebilirler. Endoskopik ultrasonografi invasyonun derinliğini göstermekte %90, bölgesel lenf nodu tutulumunu göstermekte ise %80 güvenilirdir. Göğüs kafesi ve karının tomografi ile taranması akciğer ve karaciğer metastazlarını gösterebilir ama evreleme konusunda işe yaramaz. Laparaskopi evrelemede ve rezeksiyon şansını göstermede güvenilir olarak daha sık kullanılmaya başlanmıştır.
Mide kanserinin standart tedavisi hastalığın gross ve mikroskopik olarak var olduğu bölgelerin cerrahi olarak rezeksiyonudur. Ameliyet sonrası lokalbölgesel tekrarlama oranı %80’dir. Ameliyat sonrası kemoterapi ve radyoterapi eklenmesi lokal rekürens oranlarını düşürür ve küratif rezeksiyon yapılan hastalarda sağkalımı uzatır. ABD’de hastaların üçte ikisinde ilerlemiş hastalık görülür (III. ve IV. Evre) ve sağ kalım oranı %5 'ten düşüktür. Bu hastalarda tedavinin başlıca bileşeni kemoterapidir ama uzun süreli sağ kalım nadirdir. Tıkanma ve kanamayı önlemek için palyatif rezeksiyon yapılabilir; bazı hastalarda radyoterapi ve endoskopi de palyatifyarar sağlayabilir. Gastrik lenfomalarda tedavi seçenekleri hastalığın evresine bağlı olarak kemoterapi, radyoterapi, ve/veya cerrahi tedavi kombinasyonları olabilir.
Kolon ve rektum kanseri Amerika’da kadın ve erkeklerde en sık görülen 3. kanser türüdür ve kanser nedeni ile ölümlerin 2. nedenidir. 2006 yılında 148.610 yeni vaka ve 55.170 kolorektal kansere bağlı ölüm beklenmektedir. Hem erken tanı koyma suretiyle mortalitede hem de premalign adenamların saptanması ve rezeksiyonu ile insidansta bir azalmaya yol açması bakımından tarama etkili bir stratejidir.
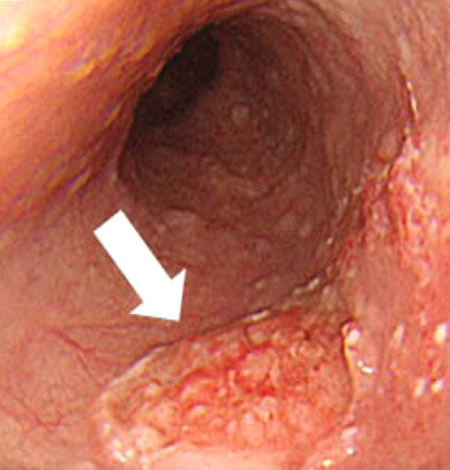
Dünyada kolorektal kanserin insidansı ve mortalitesi farklılık göstermektedir. Japonya’yı özellikle dışarıda tutmak koşulu ile en yüksek risk endüstrileşmiş ülkelerde görülmektedir. ABD’de insidans oranları son on yılda hafifçe azalmakla birlikte hala yüz binde kırk gibi yüksek bir orandadır. Amerikalılar için ömür boyu görülme oranı %6 dır. Yaş risk için önemli bir göstergedir. Otuz beş yaşından önce çok nadir görülse de (alttayatan nadir genetik sendromlar dışında), kolorektal kanser 40 yaşlarında başlar, insidansı yaş la sürekli olarak ve 80 yaşına kadar her on yılda ikiye katlanarak artar. Rektum kanseri erkeklerde daha sık görülürken kolon kanserinin görülme oranı erkek ve kadınlarda benzerdir. Zencilerde ıV. Evre hastalık insidansı hafifçe daha yüksek olsa da kolorektal kanserler geneııikle ırk farkı gözetmez. Kolorektal kanserler için önemli sayıda değiştirilebilir risk faktörü olduğu epidemiyolojik çalışmalarla gösterilmiştir. Hastalık riskini artıran faktörler, obezite, kırmızı et ve alkol tüketimi ve tütün kuııanımıdır. Riski azaltan faktörler ise fiziksel aktivite, bazı sebzelerin tüketimi ve folik asit içeren multivitaminlerdir. Kolorektal kanserIerin çoğu benign adenomatöz poliplerden (adenamlardan) köken alır. Kolorektal adenamların epidemiyolojik etkenIeri kolorektal kanserlerinki ile benzerdir. Genelde, kolorektal adenam prevalansı aynı ülkedeki kolorektal kanser prevalansı ile paraleııik gösterir. Yüksek riskli ülkelerde yaş önemli bir göstergedir. ABD’ de otopsi çalışmalarının gösterdiğine göre, tüm vakaların prevalansı %50 dir. Bu oran 50 yaşlarında yaklaşık %30 iken, 80 yaşında %55’e varır. Neyse ki adenamların sadece çok azı kolorektal kansere dönüşür. Bir adenomun invasiv kansere dönüşümü için geçen süre bilinmemektedir fakat birçok gözlemsel çalışmanın bulgularına göre bu süre en az 10 yıldır. Adenokarsinom gelişiminden sorumlu moleküler mekanizmaların incelenmesi göstermiştir ki kolorektal karsinogenez çok aşamalı bir süreçtir.
Bu süreç çeşitli onkojenlerin katılımı ile genetik değişimIerin meydana gelmesi, (örneğin K-ras), tümor supresör genler (örneğin APC veya b-Catenİn, DCC, SMAD4, SMAD2, p53) ve bazen DNA uyumsuz tamir genleri (örneğin: hMLH1) ile ilgilidir. Tanımlanmış olan yüksek risk gruplarında ailesel ya da kişisel adenamlar veya kolorektal kanser, polipoz olan ya da olmayan genetik sendromlar ve enflamatuar barsak hastalığı öyküsü vardır. Herediter nonpolipoz kolorektal kanser (HNPCC) ve ailesel adenomatöz polipoz (FAP) kolorektal kanser için en yüksek risk taşıyan genetik sendromlar olarak bilinirler. HNPCC (Lynch Sendromu), DNA Mismatch Repair genlerinden birinin aktarılmış mutasyonları, polipaz yokken erken başlangıçlı kolorektal kanser (ortalama 44 yaş), splenik fleksuranın proksimalindeki tümörlerin predominansı (%60-70), hem kolorektal ve hem de kolon dışı kanserlerin (örneğin endometrium) fazlalığı, ve yaşam boyu kolorektal kanser riskinin %80-90 olmasıile karakterizedir. Bunun aksine, FAP aktarılnuş APC gen mutasyonları, 20’li 30’lu yaşlarda yüzlerce kolorektal adenam görülmesi ve tedavi edilmez ise 50’li yaşlarda kolorektal kanser riskinin %100’lere varması ile karakterizedir. FAP, midedeki benign fundus gland polipleri, duodenal adenomlar, ve periampuller bölgeyi tutma eğiliminde olan adenokarsinomlar ile ilişkilidir. Gardner’s sendromu etkilenen probandların osteomalar, dezmoidler ve diğer yumuşak doku tümörleri gibi çok çeşitli barsak dışı tutulumlar gösterdiği bir FAP varyantıdır. Retinal pigment epitelinin konjenital hipertrofisi hem FAP hem de Gardner’s sendromu için erken benign bir durumdur. FAP’ dan ayrıştırılamayan MYH-associated Adenomatöz Polipozis Sendromu APC’ den daha çok temel eksizyon repair gende ve mutY homoloğunda (MYH) mutasyonlarla ilişkilidir. Peutz-Jeghers sendromu ince ve kalın barsakta hamartamöz polipozlar ve mukokütanöz pigmentasyon ile karakterizedir. Peutz-Jeghers sendromu olan kişiler genç yaşta hem gastrointestinal (mide, ince barsak, kolon) hem de barsak dışı (örneğin genital sistem, pankreas, meme) maligniteleri için yüksek risk grubundadırlar. leneralize Juvenil Polipozis kolorektal kanser için küçük bir risk oluşturan bir diğer kalıtımsal hamartamöz polipaz sendromudur.
Kolorektal neoplazmların çoğunluğu ileri aşamaya gelene kadar asemptomatiktir. En sık semptom gastrointestinal kanamadır ve gizli kanama, hematokezya veya açıkIanamayan demir eksikliği anemisi olarak ortaya çıkabilir. Diğer semptomlar; tıkanma ya da invazyon nedeni ile karın ağrısı, barsak alışkanlıklarında değişiklik ve açıklanamayan iştahsızlık ve kilo kaybıdır. İlerlemiş çekum kanserlerinde palpe edilen bir kitle olabilir.
Kolorektal neoplazm düşündüren semptomu olan tüm hastalarda kolon kolonoskopi ile değerlendirilmelidir. Asemptomatik ve orta risk grubundaki hastalar elli yaşından itibaren gaitada gizli kan, fleksibl sigmoidoskopi, baryum veya kolonoskopi ile periyodik olarak taramadan geçirilmelidir. Bilgisayarlı tomografi ile kolografi (virtual kolonoskop) ve gaita ile DNA testi ümit vaad eden yeni tarama stratejileridir ama otoriteler tarafından henüz kabul görmektedir. Yüksek riskli hastalarda tarama önerileri risk faktörlerine göre değişiklik göstermektedir fakat genellikle orta risk grubunda olanlarda daha erken yaşta kolonoskopi yapılması ve daha sık aralıklarla tarama esasına dayanır. Kolorektal kanser, adenam ya da inflamatuar barsak hastalığı öyküsü olanlarda kolonoskopik takip önerilir. Kolorektal kanser ve adenamların %50’ den fazlası rektum ve splenik fleksura arasında yerleşir; bununla birlikte, splenik fleksuranın proksimalinde yer alan kanserlerin prevalansı yaşla, özellikle de kadınlarda artar. Kolorektal kanserler sapsız [düz] ya da pedünküle [bir sap üzerinde] polipler şeklinde olabilir veya bir darlık, mantar gibi büyüyen kitleler veya ülsere bir kitle şeklinde ortaya çıkabilir. Kolonoskopi hem küçük polipler ve erken
kanserleri görme hem de işlem sırasında biyopsi alma ya da kanserli lezyonları temizleme olasılıkları açısından baryumlu tetkiklerden daha değerlidir. Baryumla tespit edilen lezyonların kolonoskopi ile değerlendirilmeleri gereklidir. Karın ve pelvisin bilgisayarlı tomografi ile taranması preoperatif olarak hastalığın metastatik yayılımını değerlendirmek için kullanılır. EUS rektal kanserin preoperatif evrelenmesinde kullanılır. Karsinoembriyojenik antijen düzeyi preoperatif bir ilk değer olarak ölçülür
ve eğer yüksekse postoperatif olarak tümör rekürrensinin değerlendirilmesi için takip edilir.
Kolorektal karsinomalı hastaların sağkalım oranı hastalığın evresine göre değişir. (Tablo 38-3) maalesef hastaların %45’i hastalığın 3. ya da 4. evresinde ilk muayeneye gelir. Erken dönem kolorektal kanserlerde cerrahi tek başına küratiftir. Evre 3 kolon kanserleri için cerrahi ve 5-fluorouracil ve lökovorin ile adjuvan kemoterapi önerilmektedir. Evre 2 ve 3 rektal kanserli hastalar için postoperatif radyasyon ile birlikte 5 fluourasil (Iökovorin eklenebilir ya da eklenmeyebilir) kombinasyonunun tekrarlama oranını, kansere bağlı ölümleri ve tüm mortaliteyi belirgin oranda azalttığı bulunmuştur. Dördüncü evredeki hastalar için, palyatif cerrahi, kemoterapi ve/veya radyoterapi tedavinin ana unsurlarıdır.
ABD’de karsinoid tümörlerin insidansı yüzbinde 1-2’ dir. En sık yerleşim yerleri, sıklığa göre sırayla, appendiks, ileum, rektum, bronş, mide ve kolondur. Karsinoid tümörler nöroendokrin hücrelerden köken alır ve değişik hormonlar ve biyojenik aminler içeren salgısal granüııeri vardır. Serotonin 5-hidroksitriptofandan sentezlenir ve karaciğerde biyolojik olarak inert olan ve idrarla atılan 5-hidroksi indolasetik asite metabolize olur.Serotonin (hindgut tümörleri) ve diğer vazoaktif maddelerin sistemik dolaşıma salınmasının karsinoid sendroma neden olduğu düşünülmektedir. Böylece karaciğer ya da sistemik venIere direne olan diğer bölgelerin karsinoid metastazları karsinoid sendrom la ilişkili olabilir. Bu durumda primer karsinoidier ovaryum ya da bronşlar da olabilir. Semptomlar epizodik flushing, vizing, diyare, sağ ventrikül kalp kapak hastalığı ve potansiyel olarak vasomotor kollaps olabilir. Lokalize tümörler yerlerine bağlı olarak aşırı ya da gizli kanamaya, tıkanma semptomlarına veya karın ağrısına neden olabilirler. Karsinoidlerin çoğu sessizdir ama malignite potansiyeııeri farklı olabilir ve lokalizasyonu ve primer tümörün büyüklüğü ile ilişkili gibi görünmektedir. ileumda ortaya çıkan ve 2 cm. ya da daha büyük olan karsinoidIer en büyük malignite potansiyeline sahip olanlardır. Karsinoid tümörler için tek küratif tedavi cerrahi rezeksiyondur. Somatostatin analogları karsinoid sendrom semptomları üzerinde çok etkilidir.